Nesen Ķīnas Valsts pārtikas un zāļu pārvalde (SFDA) oficiāli apstiprināja tafolecimaba (PCSK-9 monoklonālās antivielas, ko ražo INNOVENT BIOLOGICS,INC), INC, tirdzniecības pieteikumu primārās hiperholesterinēmijas (tostarp heterozigotas ģimenes hiperholesterinēmijas un nepārmantotas hiperholesterinēmijas) un jauktas dislipidēmijas ārstēšanai. Šis ir pirmais pašražotais PCSK-9 inhibitors, kas pieteikts tirdzniecībai Ķīnā.
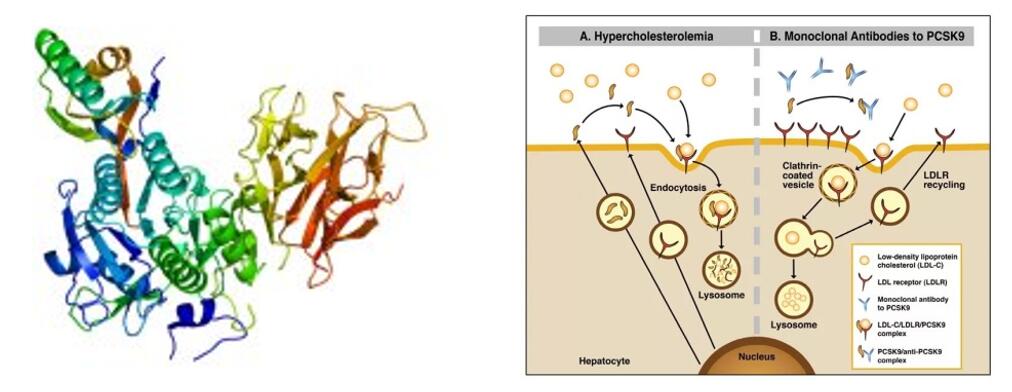
Tafolecimabs ir inovatīvs bioloģisks medikaments, ko neatkarīgi izstrādājusi INNOVENT BIOLOGICS, INC. IgG2 cilvēka monoklonālā antiviela specifiski saistās ar PCSK-9, lai palielinātu ZBL receptoru (ZBLR) līmeni, samazinot PCSK-9 mediēto endocitozi, tādējādi palielinot ZBL holesterīna elimināciju un pazeminot ZBL holesterīna līmeni.
Pēdējos gados dislipidēmijas izplatība Ķīnā ir ievērojami palielinājusies. Dislipidēmijas un hiperholesterinēmijas izplatība pieaugušajiem sasniedz attiecīgi 40,4% un 26,3%. Saskaņā ar 2020. gada ziņojumu par sirds un asinsvadu veselību un slimībām Ķīnā, dislipidēmijas ārstēšanas un kontroles līmenis pieaugušajiem joprojām ir zems, un dislipidēmijas pacientu ZBL holesterīna līmeņa ievērošanas līmenis ir vēl mazāk apmierinošs.
Iepriekš statīni bija galvenā hiperholesterinēmijas ārstēšanas metode Ķīnā, taču daudziem pacientiem joprojām neizdevās sasniegt ārstēšanas mērķi – ZBL holesterīna līmeņa samazināšanu pēc ārstēšanas. PCSK-9 laišana tirgū ir nodrošinājusi labāku efektivitāti pacientiem.
INNOVENT BIOLOGICS, INC iesniegtais tafolecimaba pieteikums ir balstīts uz trīs klīnisko pētījumu rezultātiem, kas reģistrēti demokrātiskā posmā. Tam ir labs kopējais drošības profils, kas ir līdzīgs tirgū laisto produktu drošības raksturlielumiem, un tas ir sasniedzis garus lietošanas intervālus (ik pēc 6 nedēļām). CREDIT-2 pētījuma rezultāti tika pieņemti Amerikas Kardioloģijas koledžas (ACC) 2022. gada ikgadējā sanāksmē kā kopsavilkums un publicēti tiešsaistē.
Ja pieteikums tiks apstiprināts, tas pārtrauks strupceļu PCSK-9 ieviešanas jautājumā, Ķīnai kļūstot par ceturto valsti, kurā ir PCSK-9, pēc Amerikas Savienotajām Valstīm (Amgen), Francijas (Sanofi) un Šveices (Novartis).
Publicēšanas laiks: 2022. gada 4. jūlijs