Nylig godkjente det kinesiske mat- og legemiddeltilsynet (SFDA) offisielt markedsføringssøknaden for tafolecimab (PCSK-9 monoklonalt antistoff produsert av INNOVENT BIOLOGICS,INC), INC for behandling av primær hyperkolesterolemi (inkludert heterozygot familiær hyperkolesterolemi og ikke-familiær hyperkolesterolemi) og blandet dyslipidemi. Dette er den første egenproduserte PCSK-9-hemmeren som har søkt om markedsføring i Kina.
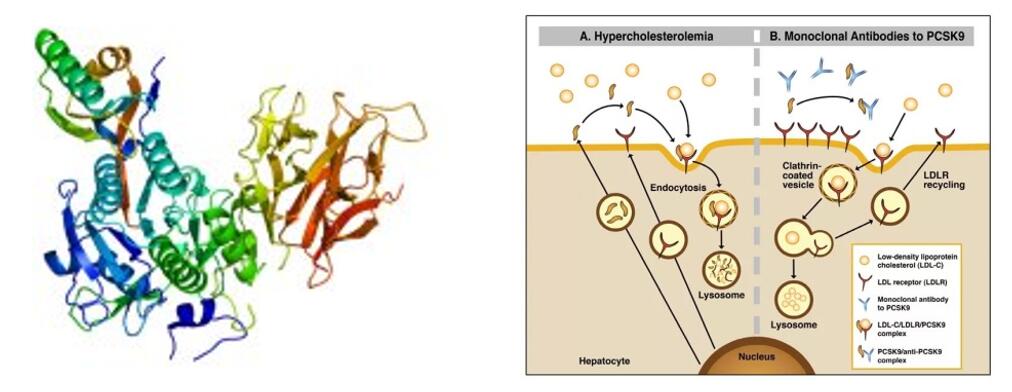
Tafolecimab er et innovativt biologisk legemiddel uavhengig utviklet av INNOVENT BIOLOGICS, INC. IgG2 humant monoklonalt antistoff binder seg spesifikt til PCSK-9 for å øke LDLR-nivåene ved å redusere PCSK-9-mediert endocytose, og dermed øke LDL-C-eliminering og senke LDL-C-nivåene.
I de senere årene har forekomsten av dyslipidemi økt betydelig i Kina. Forekomsten av dyslipidemi og hyperkolesterolemi hos voksne er så høy som henholdsvis 40,4 % og 26,3 %. I følge rapporten om kardiovaskulær helse og sykdommer i Kina fra 2020 er behandlings- og kontrollraten for dyslipidemi hos voksne fortsatt på et lavt nivå, og LDL-kolesterol-compliance-raten for dyslipidemipasienter er enda mindre tilfredsstillende.
Tidligere var statiner hovedbehandlingen for hyperkolesterolemi i Kina, men mange pasienter klarte fortsatt ikke å oppnå behandlingsmålet om reduksjon av LDL-kolesterol etter behandling. Markedsføringen av PCSK-9 har gitt bedre effekt for pasientene.
Innsendingen av tafolecimab fra INNOVENT BIOLOGICS, INC er basert på resultatene fra tre kliniske studier registrert i en demokratisk fase. Den har en god generell sikkerhetsprofil, lik sikkerhetsegenskapene til markedsførte produkter, og har oppnådd lange administreringsintervaller (hver 6. uke). Resultatene fra CREDIT-2-studien ble akseptert av det årlige møtet til American College of Cardiology (ACC) i 2022 som et sammendrag og publisert på nett.
Hvis søknaden blir godkjent, vil den bryte den fastlåste situasjonen med den improviserte PCSK-9, og Kina vil bli det fjerde landet som har PCSK-9 etter USA (Amgen), Frankrike (Sanofi) og Sveits (Novartis).
Publisert: 04.07.2022