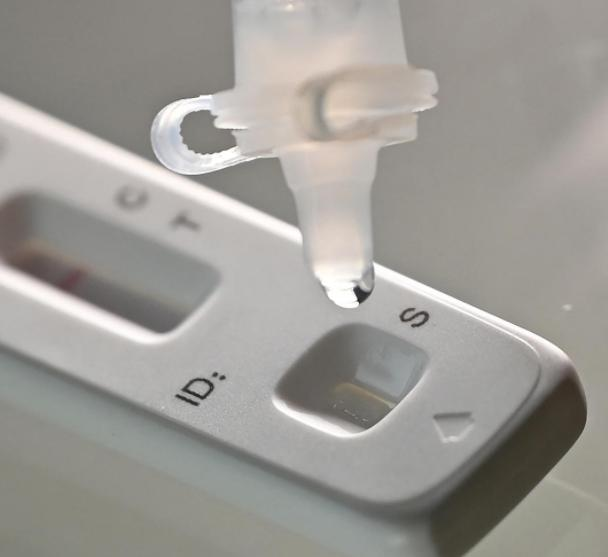
12. marsth 2022, deNMPA (SFDA) utstedte en kunngjøring som godkjenner endringen av søknaden om selvtesting av COVID-19-antigenprodukter fra Nanjing Vazyme BiotechCo., Ltd., Beijing Jinwofu bioingeniørteknologiCo., Ltd., Shenzhen Huada Yinyuan farmasøytisk teknologi Co., Ltd., Guangzhou Wondfo Biotech Co., Ltd. ogBEijing Savant Biotechnology Co., Ltd.(Huaketai)Fem produkter for selvtesting av COVID-19-antigen er lansert.
11. mars 2022 kunngjorde NHC at for å optimalisere teststrategien for det nye koronaviruset ytterligere og imøtekomme behovene for forebygging og kontroll av COVID-19, bestemte det omfattende teamet i den felles forebyggings- og kontrollmekanismen i statsrådet å legge til antigentesting i tillegg til nukleinsyretesting og utarbeidet «applikasjonsprotokollen for påvisning av antigen for deteksjon av nye koronavirus (studie)».
Protokollen spesifiserer den aktuelle populasjonen for antigentesting:
Først de som oppsøker primærmedisinske institusjoner og har symptomer som luftveisinfeksjoner og feber innen 5 dager etter symptomdebut;
For det andre, personell i karanteneobservasjon, inkludert observasjon av hjemmekarantene, nærkontakt og subnærkontakt, observasjon av inngangskarantene, personell i inneslutnings- og kontrollområder;
Den tredje er innbyggerne i lokalsamfunnet som har behov for egendeteksjon av antigen.
Tips: Antigendeteksjon er et viktig supplement til nukleinsyredeteksjon, men resultatene av antigen-selvdeteksjon kan ikke brukes som grunnlag for diagnose av infeksjon.
Publisert: 22. mars 2022