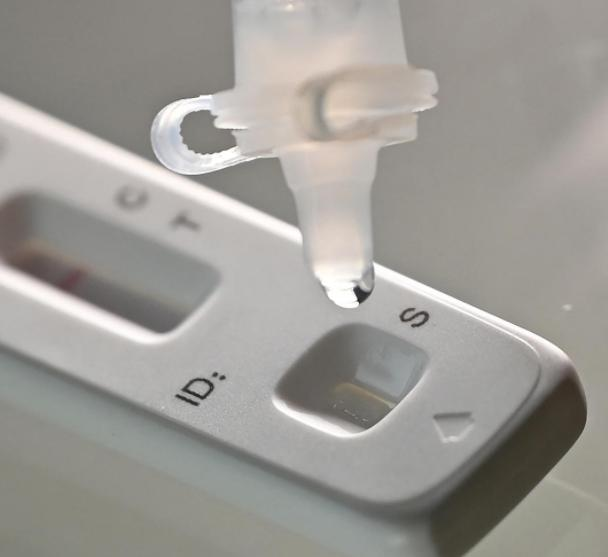
12 marcath 2022 roku tenNMPA (SFDA) wydała zawiadomienie zatwierdzające zmianę wniosku o samotestowanie produktów antygenowych COVID-19 przez Nanjing Vazyme BiotechSpółka z ograniczoną odpowiedzialnością, Beijing Jinwofu Bioengineering TechnologySpółka z ograniczoną odpowiedzialnością, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd IBeijing Savant Biotechnology Co.,ltd(Huaketai)Wprowadzono na rynek pięć produktów do samodzielnego testowania antygenów COVID-19.
11 marca 2022 r. Narodowy Komitet Zdrowia (NHC) ogłosił, że w celu dalszej optymalizacji strategii testowania nowego koronawirusa i zaspokojenia potrzeb w zakresie zapobiegania i kontroli COVID-19, Kompleksowy Zespół Wspólnego Mechanizmu Zapobiegania i Kontroli Rady Państwa podjął decyzję o dodaniu testów antygenowych do testów kwasu nukleinowego i opracował „Protokół Aplikacyjny dla Wykrywania Antygenu Nowego Koronawirusa (Trial)”.
Protokół określa populację, dla której można wykonać badanie antygenowe:
Po pierwsze, osoby, które zgłaszają się do placówek podstawowej opieki zdrowotnej i w ciągu 5 dni od wystąpienia objawów mają takie objawy, jak problemy z oddychaniem i gorączka;
Po drugie, personel nadzorujący kwarantannę, w tym personel nadzorujący kwarantannę domową, personel nadzorujący bliski i podbliski kontakt, personel nadzorujący kwarantannę wjazdową, personel obszaru zamkniętego i obszaru kontrolnego;
Trzecią grupą są mieszkańcy danej społeczności, którzy mają potrzebę samodzielnego wykrywania antygenów.
Wskazówki: Wykrywanie antygenów jest ważnym uzupełnieniem wykrywania kwasów nukleinowych, ale wyniki samodetekcji antygenów nie mogą być podstawą diagnozy zakażenia
Czas publikacji: 22 marca 2022 r.