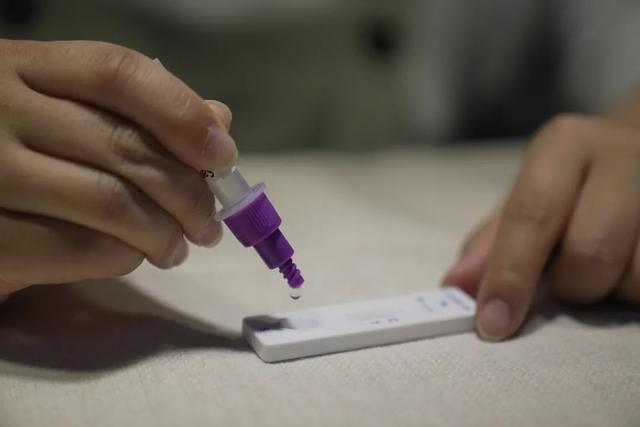
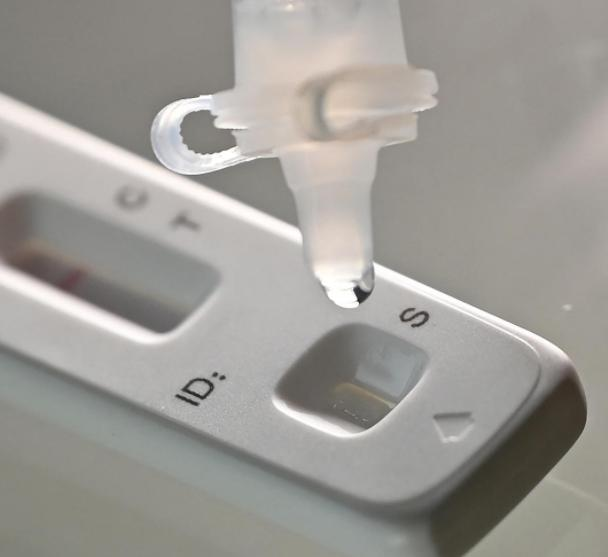
Noong Marso 12th 2022, angNMPA (SFDA) naglabas ng notice na nag-aapruba sa pagbabago ng aplikasyon para sa self-test ng mga produktong antigen ng COVID-19 ng Nanjing Vazyme BiotechCo., Ltd, Beijing Jinwofu Bioengineering TechnologyCo., Ltd, Shenzhen Huada Yinyuan Pharmaceutical Technology Co., Ltd, Guangzhou Wondfo Biotech Co., Ltd atBeijing Savant Biotechnology Co.,ltd(Huaketai). Limang COVID-19 antigen self-testing na produkto ang inilunsad.
Noong ika-11 ng Marso 2022, inanunsyo ng NHC na, upang higit pang ma-optimize ang diskarte sa pagsusuri ng Novel Coronavirus at maibigay ang mga pangangailangan ng pag-iwas at pagkontrol sa COVID-19, ang Comprehensive Team ng Pinagsanib na mekanismo ng pag-iwas at pagkontrol ng Konseho ng Estado ay nagpasya na magdagdag ng pagsusuri ng antigen sa pagsusuri ng nucleic acid at ginawa ang "Application Protocol para sa Novel Coronavirus Antigen Detection (Trial)"
Tinukoy ng protocol ang naaangkop na populasyon para sa pagsusuri ng antigen:
Una, ang mga bumibisita sa mga pangunahing institusyong medikal at may mga sintomas tulad ng respiratory tract at lagnat sa loob ng 5 araw mula sa pagsisimula ng mga sintomas;
Pangalawa, quarantine observation personnel, kabilang ang home quarantine observation, close contact at sub-close contact, entry quarantine observation, containment area at control area personnel;
Ang pangatlo ay ang mga residente ng komunidad na nangangailangan ng antigen self-detection.
Mga Tip:Ang antigen detection ay isang mahalagang suplemento ng nucleic acid detection, ngunit ang mga resulta ng antigen self-detection ay hindi magagamit bilang batayan para sa diagnosis ng impeksyon
Oras ng post: Mar-22-2022